 Número atómico: 18
Número atómico: 18Grupo: 18
Periodo: 3
Configuración electrónica: [Ne] 3s2 3p6
Estados de oxidación: 0
Electronegatividad: -
Radio atómico / pm: 188
Masa atómica relativa: 39.948 ± 0.001
El argón fue descubierto en 1894 por los científicos británicos sir William Ramsay y John William Strutt Rayleigh. Por la pasividad química que le caracteriza recibió su nombre, del griego 'argos', que significa inactivo. Es gas noble, incoloro, inodoro e insípido. En la naturaleza se encuentra en el aire atmosférico, del que constituye aproximadamente el 1 % en volumen. Su aplicación más importante es la de gas protector en la soldadura eléctrica del acero y para llenar lámparas de incandescencia, dando iluminación azulada.
PROPIEDADES FISICAS
Densidad / g dm-3: 1656 (40 K)
1.784 (273 K)
Volumen molar / cm3mol-1: 24.12 (40 K)
22392.38 (273 K)
Resistencia eléctrica / μΩcm: - (20 °C)PROPIEDADES TÉRMICAS
Conductividad térmica / W m-1K-1: 0.0179Punto de fusión / °C: -189.34
Punto de ebullición / °C: -185.89
Calor de fusión / kJ mol-1: 1.21
Calor de vaporización / kJ mol-1: 6.53
Calor de atomización / kJ mol-1: 0
ENERGÍA DE IONIZACIÓN
Primera energía de ionización / kJ mol-1: 1520.58Segunda energía de ionización / kJ mol-1: 2665.88
Tercera energía de ionización / kJ mol-1: 3930.84
ABUNDANCIA DE ELEMENTOS
en la atmósfera / ppm : 9300en la corteza terrestre / ppm: 1.2
en los océanos / ppm: 0.6
DATOS CRISTALOGRÁFICOS
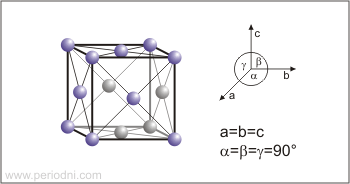 Estructura cristalina:
Estructura cristalina:
cúbica centrada en las caras
Dimensiones de la celda unidad / pm:
a=531.088
Grupo espacial:
Fm3m
ISÓTOPOS
Isótopo Masa atómica relativa Porcentaje por masa (%)
36Ar 35.9675463(3) 0.337(3)
37Ar 36.9667759(3) *
38Ar 37.9627322(5) 0.063(1)
39Ar 38.964313(5) *
40Ar 39.962383123(3) 99.600(3)